Unit 7 Stoichiometry Mole Conversion Worksheet: A Comprehensive Guide delves into the fascinating world of stoichiometry, unveiling the intricate relationship between moles, mass, and chemical reactions. This in-depth exploration provides a solid foundation for understanding the quantitative aspects of chemistry, empowering students to navigate complex chemical calculations with precision and confidence.
Stoichiometry, the study of the quantitative relationships between reactants and products in chemical reactions, plays a pivotal role in various scientific disciplines. It enables scientists and engineers to predict the outcome of chemical reactions, design experiments, and develop new technologies.
This worksheet serves as a valuable tool for mastering stoichiometric principles, equipping students with the skills to tackle real-world chemistry challenges.
Unit 7 Stoichiometry: Unit 7 Stoichiometry Mole Conversion Worksheet
Stoichiometry adalah cabang kimia yang mempelajari kuantitas relatif reaktan dan produk dalam reaksi kimia. Konsep ini sangat penting untuk memahami dan memprediksi hasil reaksi kimia.
Salah satu konsep dasar dalam stoichiometry adalah mol. Mol adalah satuan pengukuran yang digunakan untuk menyatakan jumlah suatu zat. Satu mol suatu zat didefinisikan sebagai jumlah zat yang mengandung jumlah entitas elementer (atom, molekul, ion, atau elektron) yang sama dengan jumlah atom dalam 0,012 kilogram karbon-12.
Mol memiliki peran penting dalam perhitungan stoikiometri karena memungkinkan kita untuk menghubungkan massa suatu zat dengan jumlah entitas elementernya. Hubungan ini dinyatakan dalam rumus massa molar, yang didefinisikan sebagai massa satu mol suatu zat.
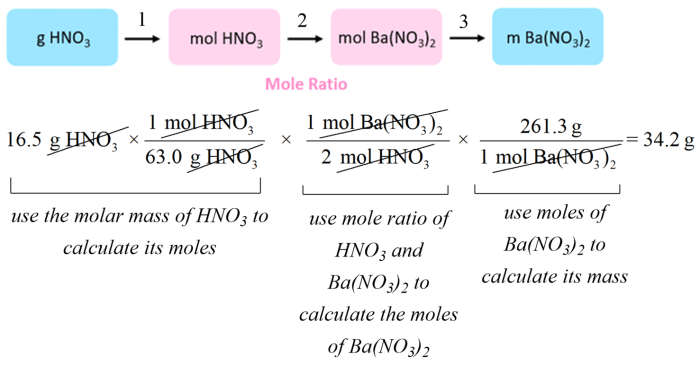
Mole Conversions
Konversi mol adalah proses mengubah jumlah suatu zat dari satu satuan pengukuran ke satuan pengukuran lainnya. Konversi ini dapat dilakukan menggunakan rumus massa molar zat tersebut.
Berikut adalah langkah-langkah yang terlibat dalam melakukan konversi mol:
- Tentukan massa zat dalam gram.
- Bagi massa zat dengan massa molarnya untuk mendapatkan jumlah mol.
- Kalikan jumlah mol dengan faktor konversi yang sesuai untuk mendapatkan jumlah zat dalam satuan yang diinginkan.
Stoichiometry Worksheet, Unit 7 stoichiometry mole conversion worksheet
Lembar kerja stoikiometri dirancang untuk membantu siswa melatih keterampilan konversi mol mereka. Lembar kerja ini biasanya berisi berbagai masalah yang mengharuskan siswa untuk mengubah jumlah zat dari satu satuan pengukuran ke satuan pengukuran lainnya.
Untuk menyelesaikan masalah dalam lembar kerja stoikiometri, siswa perlu mengikuti langkah-langkah berikut:
- Baca soal dengan cermat dan identifikasi zat yang terlibat.
- Tentukan massa zat yang diberikan dalam soal.
- Cari massa molar zat tersebut.
- Gunakan rumus konversi mol untuk mengubah massa zat menjadi jumlah mol.
- Gunakan koefisien stoikiometri dalam persamaan reaksi untuk menentukan jumlah mol zat lainnya yang terlibat dalam reaksi.
- Konversi jumlah mol zat lain ke satuan yang diinginkan.
Real-World Applications
Stoichiometry memiliki banyak aplikasi di dunia nyata, termasuk:
- Dalam kedokteran, stoikiometri digunakan untuk menentukan dosis obat yang tepat untuk pasien.
- Dalam teknik, stoikiometri digunakan untuk merancang dan mengoptimalkan proses kimia.
- Dalam ilmu lingkungan, stoikiometri digunakan untuk memahami dan memprediksi dampak aktivitas manusia terhadap lingkungan.
Additional Resources
Berikut adalah beberapa sumber tambahan yang dapat membantu Anda mempelajari lebih lanjut tentang stoikiometri:
- Buku: “Chemistry: The Central Science” oleh Theodore L. Brown, H. Eugene LeMay, Jr., Bruce E. Bursten, dan Catherine J.
Murphy
- Situs web: Khan Academy (https://www.khanacademy.org/science/chemistry/chemical-reactions/stoichiometry/a/stoichiometry)
- Video: Crash Course Chemistry (https://www.youtube.com/watch?v=2Zrk7gB1uRU)
Detailed FAQs
What is stoichiometry?
Stoichiometry is the study of the quantitative relationships between reactants and products in chemical reactions.
What is a mole?
A mole is a unit of measurement that represents a specific number of particles (atoms, molecules, or ions) of a substance. One mole is equal to 6.022 × 10^23 particles.
How are moles used in stoichiometric calculations?
Moles are used to convert between the mass and number of particles of a substance, enabling the determination of reactant and product quantities in chemical reactions.